
以无机物资制备为载体的概括型执行迷奸 拳交
1.气体制备与性质执行安装的聚会历程
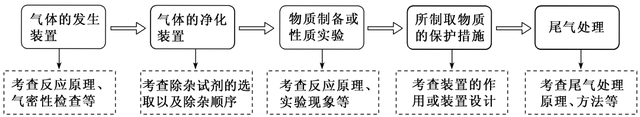
2.有气体参与的制备执行的安祥事项
(1)操作要领问题
与气体干系的执行操作要领:安装取舍与聚会气密性查验装入固体药品加液体药品按法子执行拆卸仪器
(2)加热操作的要求
①使用可燃性气体(如H2、CO、CH4等)时,先用原料气遣散系统内的空气,再燃烧乙醇灯加热,以驻防爆炸
②制备一些易与空气中的因素发生响应的物资(如H2回复CuO的执行),响应实面前,应先灭火乙醇灯,不绝通原料气至试管冷却
(3)尾气措置的口头:有毒气体常遴荐溶液(或固体)接管或将其燃烧的口头,不可径直排放
(4)迥殊执行安装
①制备在空气中易吸水、潮解以及水解的物资(如Al2S3、AlCl3等),不时在安装的结尾再接一个干燥安装,以驻防空气中水蒸气的参加
②用液体接管气体,若气体熔解度较大,要加防倒吸安装
③若制备物资易被空气中氧气氧化,应加排空气安装
④制备的物资若为液态且易蒸发时,应将集合安装置于冷水浴中
(5)冷凝回流
有些响应中,为减少易蒸发液体响应物的损耗和充分利用原料,需在响应安装上加装冷凝回流安装(如长玻璃管、冷凝管等)
3.执行要求界限的操作与看法
(1)化学执行中温度界限的看法
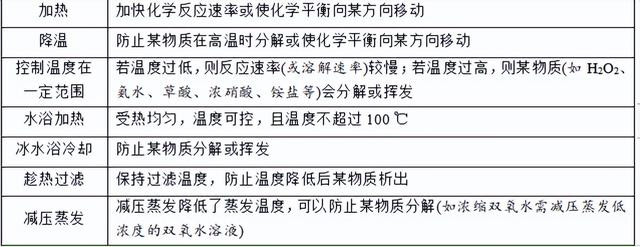
(2)执行前排空的看法
①波及可燃气体(H2、CO)的性质考证时,排空的看法是驻防可燃气体与空气搀和加热爆炸
②波及与空气中O2、CO2作用的物资,排空的看法是驻防响应物与空气中的O2、CO2响应
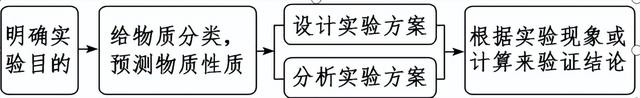
4.解无机制备类执行的想维历程

物资性质、执行旨趣的探究型概括执行
1.探究物资性质的基本口头和法子
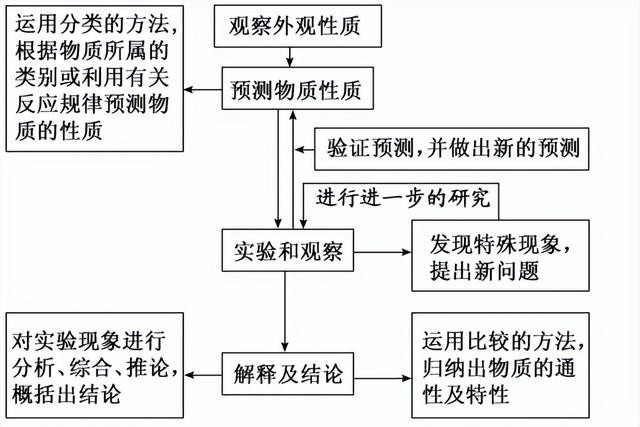
2.性质、旨趣探究类执行的设计角度分析
(1)酸性强弱比拟:可通过强酸制弱酸、对应盐溶液的碱性、同浓度溶液导电智力或pH等口头来比拟迷奸 拳交

(2)金属性强弱比拟:可通过与水或酸响应置换氢的智力、最高价氧化物对应水化物的碱性、置换响应、原电板的正负极、电解池中阴极阳离子的放电要领等口头来比拟
(3)非金属性强弱比拟:可通过最高价氧化物对应水化物的酸性、气态氢化物的安祥性、与H2化合的难易进程、互相之间的置换、对应阴离子的回复性等口头来比拟
(4)弱酸酸式盐的电离进程与水解进程比拟:可通过测定溶液的酸碱性的口头来比拟
(5)Ksp的大小比拟
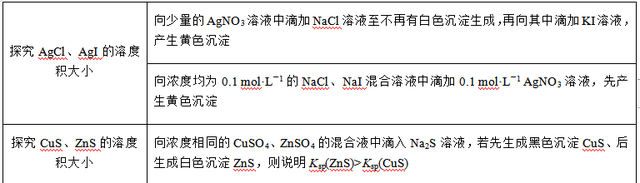
(6)一元酸、二元酸判断:可用NaOH溶液进行中庸滴定测定滥用V(NaOH)来详情
(7)羟基的数量判断:可通过取一定量试剂与足量Na响应测定放出氢气的量来详情
(8)羧基的数量判断:可通过取一定量试剂与足量NaHCO3响应测定放出CO2的量来详情
成人网有哪些3.解性质、旨趣探究类试题的想维历程
(1)第一步,明确执行看法,知谈该执行要干什么
(2)第二步,逆推执行旨趣,依据看法考虑所学常识,再邻接提给信息设计探究决议
(3)第三步,转头题干寻找对应的情境信息与执行安装,挪动诈欺所学常识,锁定探究决议
(4)第四步,合座考证分析,定谜底
物资因素或响应产物探究类概括执行
1.探究物资因素或响应产物的设计角度分析:通过化学响应旨趣揣测可能生成哪些物资,对这些物资逐一的老师来推测出究竟含有哪些物资
(1)钢铁发生电化学腐蚀的规章探究:不错通过界限钢铁是否与空气战争、所战争的电解质溶液的酸碱度、钢铁在腐蚀过程中体系内的气压变化等设计执行,找出规章

凭证物资性质,使被老师物资与加入的试剂作用,治愈为某种已知物资,或产生某种迥殊时局,从而详情该物资的存在(物资性质亦然匡助老师的进攻依据)。常见的迥殊时局有:

3.解物资因素或响应产物探究类执行题的想维历程
定量分析型概括执行
【口头与时间】
1.定量测定中的干系狡计
(1)常用的狡计公式:n=M/(m),n=22.4(V)(标况下、气体),n=cV(aq)
(2)常见的狡计类型
①物资的质料分数(或纯度)=搀和物的总质料/(该物资的质料)×100%
②居品的产率=居品的表面产量/(居品的本体产量)×100%
③物资的转变率=加入原料的总量/(参加响应的原料量)×100%
④物资构成的狡计
2.定量测定的常用口头
(1)千里淀法:先将某种因素转变为千里淀,然后称量纯洁、干燥的千里淀的质料,再进行干系狡计
(2)测气体体积法:关于产不满体的响应,不错通过测定气体体积的口头测定样品纯度。体体积的测定既可通过测量气体排出的液体体积来详情(二者体积值绝顶),也可径直测量集合的气体体积
①径直测量法
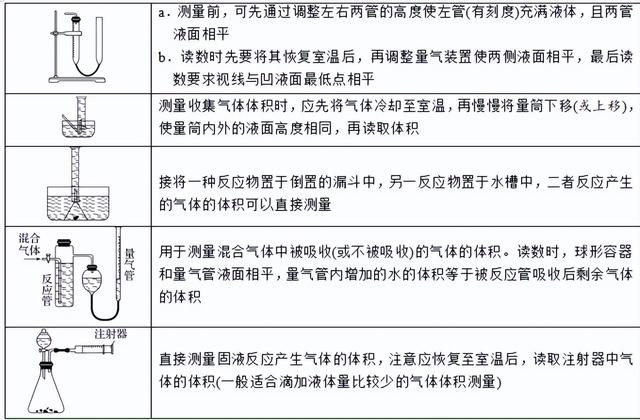
②曲折测量法:通过测量气体排出的液体体积来详情气体体积
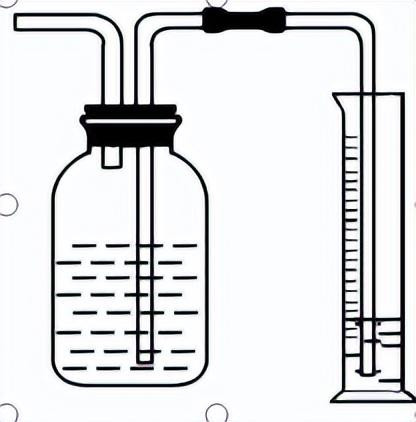
(3)测量气体质料法
①口头1:称响应安装在放出气体前后的质料减小值
②口头2:将生成的气体通入足量的接管剂中,通过称量执行前后接管剂的质料,求得所接管气体的质料,然后进行干系狡计
(4)滴定分析法:定量执行中的滴定口头包括酸碱中庸滴定、千里淀滴定、氧化回复滴定等,主若是凭证滴定过程中标准溶液的滥用量来狡计待测溶液的浓度
①类型
a.连气儿滴定法:第一步滴定响应生成的产物,还不错不绝参加第二步的滴定。凭证第二步滴定的滥用量,可狡计出第一步滴定的响应物的量
b.返滴定法:第一步用的滴定剂是过量的,第二步再用另一物资返滴定过量的物资。凭证第一步加入的量减去第二步中过量的量,即可得出第一步所求物资的物资的量
c.碘量法测定:碘量法是氧化回复滴定中应用较为昔时的一种口头。I2可作氧化剂,能被Sn2+、H2S等回复剂回复;I-可作回复剂,能被IO3-、Cr2O7(2-)、MnO4-等氧化剂氧化。碘量法分为径直碘量法和曲折碘量法,径直碘量法是用碘滴定液径直滴定回复性物资的口头,在滴定过程中,I2被回复为I-;曲折碘量法(又称滴定碘法),它是利用I-的回复性与氧化性物资响应产生I2,遇淀粉溶液显蓝色,再加入Na2S2O3标准溶液与I2响应,滴定绝顶的时局为蓝色隐匿且半分钟内不变色,从而测出氧化性物资的含量。如:用曲折碘量法测定搀和气中ClO2的含量,干系的离子方程式为2ClO2+10I-+8H+===2Cl-+5I2+4H2O和I2+2S2O3(2-)===2I-+S4O6(2-),得关系式2ClO2~5I2~10S2O3(2-),然后凭证已知要求进行狡计
②滴定执行中常用的狡计口头——关系式法
关系式法常应用于一步响应或分多步进行的连气儿响应中,利用该法不错减少无用要的中间运算过程,幸免狡计误差,并能马上准确地取得成果。一步响应不错径直找出响应物与打算产物的关系;在多步响应中,若第一步响应的产物是下一步响应的响应物,不错凭证化学方程式,将该物资看成“中介”,找出已知物资和所求物资之间量的关系。利用这种口头解题的关节是开荒已知物资和所求物资之间量的关系式
如:用Na2S2O3滴定法测水中溶氧量,经过如下三步响应:
①O2+2Mn(OH)2===2MnO(OH)2
②MnO(OH)2+2I-+4H+===Mn2++I2+3H2O
③2Na2S2O3+I2===Na2S4O6+2NaI
以永别提纯为干线的有机制备类概括执行
1.有机物制备常考的仪器、安装
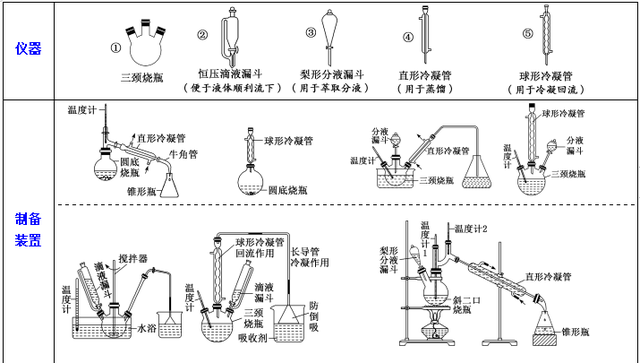
2.常见有机物的永别与提纯

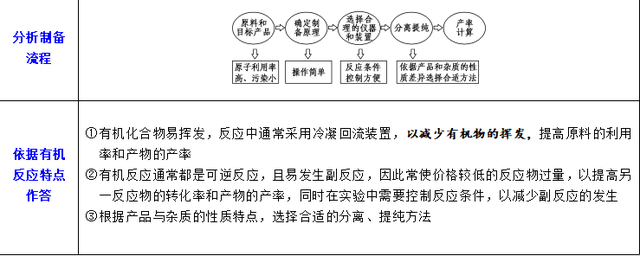
3.解有机物制备类执行的想维模子
 迷奸 拳交
迷奸 拳交
